DERIVAT ASAM KARBOKSILAT
Derivate
Asam Karboksilat
Derivate asam karboksilat adalah turunan dari asam
karboksilat, hal ini dilihat dari perubahan struktur dari pergantian gugus –OH
dalam struktur RCOOH oleh gugus NH2, -OR atau –OOCR. Terdapatnya gugus karbonil
did alam turunan asam karboksilat membuat turunannya bersifat polar, kepolaran
turunan ini berpengaruh terhadap sifat
yang ada pada turunan tersebut. Turunan asam karboksilat memiliki gugus fungsi
asil (-RCO) dan gugus fungsi aril (-ArCO). Nah, apabila turunan tersebut dihidrolisis
akan menghasilkan produk berupa asam karboksilat.
Kereaktifan
Derivat Asam Karboksilat
Suatu turunan asam karboksilat apabila dijalankan
reaksi hidrolisis akan menghasilkan produk asam karboksilat, hal ini
dipengaruhi olehnya karena mengandung gugus pergi yang tinggal, gugus
elektronegatif yang bisa hilang dan dapat hilang sebagai anion (X- atau RCO2-)
atau ini bisa berperan sebagai anion yang terprotonasi (ROH dan R2NH). Salah
satu factor kereaktifan turunan asam karboksilat yaitu pada kemudahan dalam
pembentukan intermediet tetrahedral yang dipengaruhi oleh faktor sterik dan faktor elektronik.
Macam-macam
turunan asam karboksilat
Ester
Salah satu turunan asam karboksilat ialah ester. Ester yang merupakan senyawa organic dan memiliki rumus RCOOR’. Dalam ester gugus karboksilat RCOOH yang mana –OH disini diganti dengan OR’.
Dalam pembuatan ester alkohol atau fenol direaksikan
dengan asam karboksilat yang kemudian di refluks. Reaksi pembuatan ester
dinamakan esterifikasi. Fenol yang merupakan senyawa organic yang memiliki
gugus –OH langsung mengikat pada cincin benzene. Suatu reaksi esterifikasi merupakan
reaksi yang lambat. Tetapi apabila menggunakan katalis berupa asam mineral yang
bersifat asam kuat yakni HCl dan H2SO4 reaksi kesetimbangan akan tercapai dalam
kurun waktu yang lebih singkat.
RCOOH + R’OH ↔ RCOOR’ +
H2O
Dalam esterifikasi, dimana ion H+ dari larutan H2SO4
akan berperan untuk pembentukan senyawa ester dan selain itu juga ion H+
tersebut berperan juga sebagai hidrolisis ester. Dalam pembuatan ester apabila
ingin mendapatkan rendemen ester yang tinggi maka kita harus menggeser
kesetimbangan kearah pembentukan ester.
Cepat atau tidaknya reaksi ini berjalan tergantung
kepada halangan sterik dalam alkohol, katalis, temperature dan juga konsentrasi
reaktan. Halangan sterik dalam alkohol dan juga asam karboksilat juga
mempengaruhi laju reaksinya. Dengan bertambahnya halangan sterik di dalam zat
antara, laju pembentukkan ester akan menurun. Dengan demikian rendemen ester
akan berkurang.
Kereaktifan suatu alkohol terhadap reaksi
esterifikasi dapat dilihat :
HCOOH > CH3COOH > RCH2COOH > R2CHCOOH >
R3CCOOH
REAKSI-REAKSI
ESTER
a. Reaksi
hidrolisis
Dalam pelaksanaan
reaksi hidrolisis dalam suasana asam akan menghasilkan produk berupa asam
karboksilat dan juga alkohol.
a. Reaksi
amoniak
Bila suatu ester direaksikan dengan senyawa amoniak
produk yang dihasilkan amida dan alkohol.
CH3COOC2H5 + NH3 → CH3CONH2 + C2H5OH
b. Transesterifikasi
Apabila ester direaksikan dengan alkohol produk yang
dihasilkan yaitu berupa suatu ester baru dan alkohol baru. Reaksi ini dapat
berlangsung dalam suasana asam maupun basa.
RCOOR’ + R”OH → RCOOR” + R’OH
Dalam reaksi transesterifikasi terjadi pertukaran
antara gugus alkil dimana pada –OR’ pada suatu ester dengan gugus alkil dalam R”O.
a. Pereaksi
Grignard
Apabila suatu ester direaksikan dengan pereaksi Grignard
maka akan diperoleh produk berupa alkohol tersier.
RCOOR’ + R”MgX → RCOR” + R’OMgX
Produk keton apabila direaksikan lebh lanjut bersama
R”MgX maka akan diperoleh alkohol tersier.
Permasalahan :
1.
Dalam pelaksanaan reaksi hidrolisis
ester dalam suasana asam maka akan dihasilkan produk berupa asam karboksilat. Apa
yang mungkin terjadi apabila dilakukan dalam suasan basa?.
2.
Apa yang kita lakukan apabila ingin
menda[atkan rendemen ester yang tinggi?
3.
Bagaimana bisa factor sterik dapat
mempengaruhi lajunya reaksi ester?
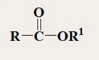





Saya Denora Situmorang (056)
BalasHapusSaya akan mencoba menjawab permasalahan no 3 menurut saya faktor sterik ini akan mempengaruhi laju reaksi dikarenakan adanya halangan sterik yang akan mempersulit untuk terjadinya reaksi sehingga untuk terjadinya pengikatan pada karbonil ada gugus pergi yang mengahalangi sehingga hal tersebut akan mempengaruhi laju reaksi. Terimakasih
Komentar ini telah dihapus oleh pengarang.
BalasHapusHai Rizki..
BalasHapusBaiklah saya Zulia Nur Rahma (A1C118048) akan menjawab permasalahan 1. Menurut saya ester yang menjalani reaksi hidrolisis dalam suasana basa dapat disebut juga dengan reaksi penyabunan atau saponifikasi. Sehingga karena reaksi berlangsung dalam suasana basa, maka yang dihasilkan ialah garam karboksilat.
Terimakasih..
Saya susilawati (A1C118091) baikalah saya akan menjawab permasalahan no 2, Sesuai dengan hukum aksi massa, untuk memperoleh rendemen ester yang tinggi maka kesetimbangan harus bergeser ke arah pembentukkan ester.
BalasHapus